Anion vs. Kation

- 3541
- 352
- Prokop Cebula
Jon jest atomem lub grupą atomów, w których liczba elektronów nie jest równa liczbie protonów, co daje dodatnie lub ujemny ładunek elektryczny netto. Jakiś anion jest jonem, który jest ujemnie naładowany i jest przyciągany do anody (elektrody dodatniej) w elektrolizy. A kation ma ładunek dodatni netto i jest przyciągany do katody (elektroda ujemna) podczas elektrolizy.
Wykres porównania
| Anion | Kation | |
|---|---|---|
| Definicja | Anion to atom lub cząsteczka, która jest ujemnie naładowana, i.mi. ma więcej elektronów niż protony. | Kation to atom lub cząsteczka, która jest dodatnio naładowana, i.mi. ma więcej protonów niż elektronów. |
| Opłata | Negatywny | Pozytywny |
| Przykłady | (O2-), siarczek (S2-), fluork (F-), chlorek (Cl-), bromek (Br-), jodek (i-), azotek (N3-) i wodorot (H-) | sód (Na+), żelazo (Fe2+) i ołów (PB2+) |
| Etymologia | Greckie słowo ano (w górę) | Greckie słowo kata (w dół) |
| Elektroda przyciągana podczas elektrolizy | Anoda | Katoda |
| Rodzaj elementu | Niemetal | metal |
Etymologia

Anion pochodzi od greckiego słowa nie, Znaczenie „up”. Słowo kation pochodzi z greckiego odpowiednika Kata, co oznacza „w dół”.
Urządzenie mnemoniczne
Dobrym sposobem zapamiętania, który typ jonów jest dodatnio naładowany, jest użycie następujących urządzeń mnemonicznych:
- Anion: A Nengatywny JON
- Kation: łapy (koty mają łapy)
Formacja ładowania
Gdy kation taki jak sód jest reprezentowany jako (Na+), ładunek „+”, który mu towarzyszy, wskazuje, że ma on o jeden elektron mniejszy niż całkowita liczba protonów. To nierównomierne równanie elektronów i protonów umożliwia sod. Podobnie, gdy anion chlorkowy jest reprezentowany z (cl-), lisowanie „” wskazuje, że ma on jeden mniej protonowy niż całkowita liczba elektronów. Jeśli znakiem „ +” lub ' -' towarzyszy liczba taka jak +4 lub -2, to oznacza, że: kation z ładunkiem +4 ma 4 mniej elektrony niż całkowita liczba protonów i anion z -2 Ładunek ma dwa mniej protonów niż całkowita liczba elektronów.
Obligacje
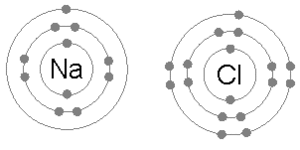 Wiązanie wiązania sodu i chloru w celu utworzenia chlorku sodu.
Wiązanie wiązania sodu i chloru w celu utworzenia chlorku sodu. W wyniku negatywnego i pozytywnego naładowania aniony i kationów zwykle tworzą wiązania. Są one znane jako wiązania jonowe i istnieją ze względu na wzajemne przyciąganie przeciwnie naładowanych jonów. Tworzą kryształową więź, w której przeciwnie naładowane jony są ze sobą związane.
Przykłady
Przykłady anionów obejmują tlenek (O2-), siarczek (S2-), fluork (F-), chlorek (Cl-), bromek (Br-), jodek (I-), azotek (N3-) i wodorot (H- ).
Przykłady kationów obejmują sód (Na+), żelazo (Fe2+) i ołów (PB2+)

