Różnica między fosforem a fosforanem
- 1756
- 233
- Prokop Cebula
Co to jest fosfor?
Fosfor (P) to wielopowodzie niemetalny element chemiczny grupy VA, bez 15 układu okresowego. Jego masa molowa wynosi 30.97. Znanych jest dwadzieścia trzy izotopy fosforu, ale tylko jeden z nich jest stabilny.

Fosfor jest elementem wysoce reaktywnym. Reaguje z tlenem, halogenami, siarką i wieloma metaliami. Ze względu na jego fosfor o wysokiej reaktywności nie można znaleźć jako wolny element na Ziemi.
Atom fosforu zawiera pięć elektronów walencyjnych na zewnętrznej warstwie. W związkach z metaliami i wodorem fosfor wykazuje stopień utleniania -3, a w interakcji z większą liczbą pierwiastków elektroonegatywnych, takimi jak tlen, fluor itp., stopnie utleniania wynoszą +3 lub +5.
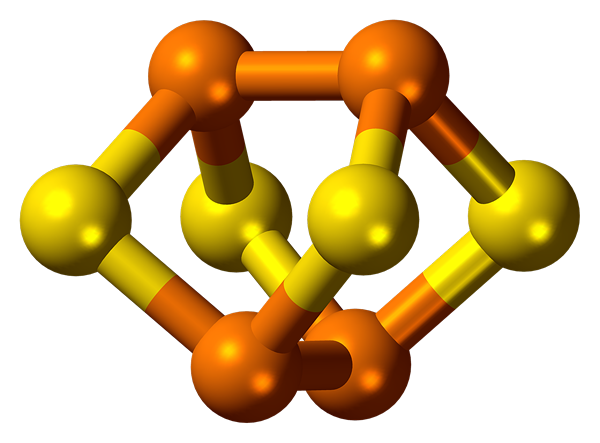
Fosfor charakteryzuje się alotropią. Tworzy kilka prostych substancji, które różnią się strukturą i właściwościami. Najczęściej rozmieszczone to fosfor biały i czerwony.
Biały fosfor składa się z p4 Cząsteczki. Jest to biała substancja podobna do wosku z żółtym odcieniem, która świeci w ciemności. Biały fosfor nie jest rozpuszczalny w wodzie, ale jest rozpuszczalny w disiarczku węgla. To jest trujące. Jest wysoce reaktywny i może spontanicznie zapalić.
Czerwony fosfor ma kryształową sieć atomową. Nie rozpuszcza się w wodzie i disiarczku węgla. Nie jest trujący i ma niższą aktywność w porównaniu z białym fosforem.
Alotropowe modyfikacje fosforu są międzykonkulantowe.
Co to jest fosforan?
Fosforan jest chemiczną pochodną kwasu fosforowego, zawierającego jon fosforanowy (PO3-4). Jon fosforanowy może tworzyć różne sole. Formalnie każda sól fosforu okacid jest fosforanem.
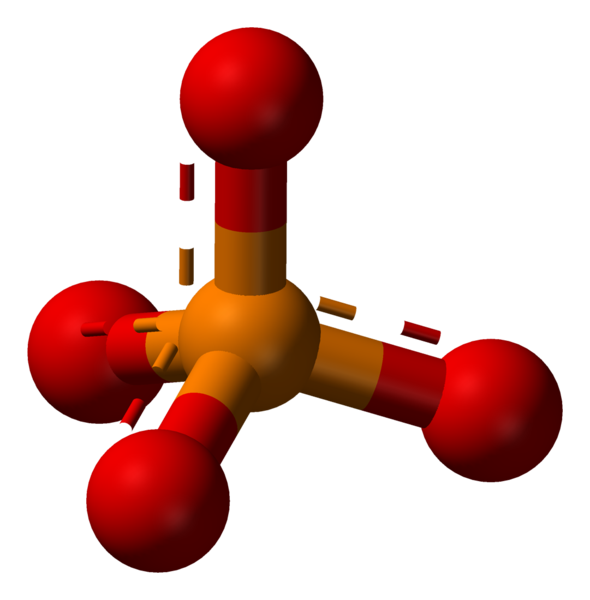
Jon fosforanowy jest jonem wielopiętrowym z czworościennym układem atomów. Składa się z jednego atomu fosforu, położonego w środku i otoczonym czterema atomami tlenu. Masa molowa jonu fosforanu wynosi 94.97 g/mol.
W zależności od liczby atomów fosforowych fosforany można podzielić na cztery główne grupy: ortofosforany, pirofosforany, tripolifosforany i polifosforany. Każda z tych grup ma swoje własne właściwości funkcjonalne.
Różnica między fosforem a fosforanem
Definicja
Fosfor: Fosfor to wielocesynne niemetalowe element chemiczny grupy VA.
Fosforan: Fosforan jest chemiczną pochodną kwasu fosforowego, zawierającego jon fosforanowy (PO3-4). Formalnie każda sól fosforu okacid jest fosforanem.
Masa cząsteczkowa
Fosfor: Masa molowa fosforu wynosi 30.97 g/mol.
Fosforan: Masa molowa jonu fosforanu wynosi 94.97 g/mol.
Wzór chemiczny
Fosfor: Symbkiem fosforu jest P.
Fosforan: Chemiczna wzór jonu fosforanowego to PO4.
Struktura
Fosfor: Fosfor tworzy kilka prostych substancji, najczęściej rozmieszczone są biały fosfor, składający się z p4 cząsteczki i czerwony fosfor, który ma kryształową sieć atomową.
Fosforan: Jon fosforanowy jest jonem wielopiętrowym z czworościennym układem atomów. Składa się z jednego atomu fosforu, położonego w środku i otoczonym czterema atomami tlenu.
Stopień utleniania
Fosfor: W związkach z metaliami i wodorem fosfor wykazuje stopień utleniania -3, a w interakcji z większą liczbą pierwiastków elektroonegatywnych, takimi jak tlen, fluor itp., Stopień utleniania wynosi +3 lub +5.
Fosforan: Fosforan wykazuje stopień utleniania -3.
Formy/typy
Fosfor: Fosfor charakteryzuje się alotropią i tworzy kilka prostych substancji, które różnią się strukturą i właściwościami. Najczęściej rozmieszczone to fosfor biały i czerwony.
Fosforan: W zależności od liczby atomów fosforu fosforany to ortofosforany, pirofosforany, tripolifosforany i polifosforany.
Fosfor vs. Fosforan: tabela porównawcza
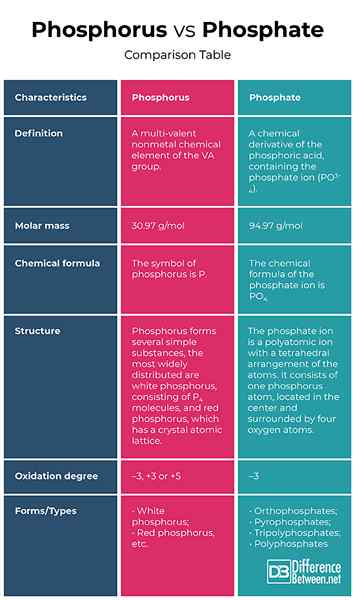
Podsumowanie fosforu vs. Fosforan:
- Fosfor to wielocesynne niemetalowe element chemiczny grupy VA.
- Fosforan jest chemiczną pochodną kwasu fosforowego, zawierającego jon fosforanowy (PO3-4). Formalnie każda sól fosforu okacid jest fosforanem.
- Masa molowa fosforu wynosi 30.97 g/mol. Masa molowa jonu fosforanu wynosi 94.97 g/mol.
- Symbkiem fosforu jest P. Chemiczna wzór jonu fosforanowego to PO4.
- Biały fosfor składa się z p4 Cząsteczki, czerwony fosfor ma kryształową sieć atomową. Jon fosforanowy jest jonem polatomowym z czworościennym układem atomów, składającym się z jednego atomu fosforowego, położonego w środku i otoczonym czterema atomami tlenu.
- Fosfor wykazuje stopień utleniania -3, +3 lub +5. Fosforan wykazuje stopień utleniania -3.
- Fosfor tworzy kilka prostych substancji, które różnią się strukturą i właściwościami, najczęściej rozmieszczone są fosfor biały i czerwony. W zależności od liczby atomów fosforu fosforany to ortofosforany, pirofosforany, tripolifosforany i polifosforany.

