Różnica między koloidem a zawieszeniem
- 1355
- 95
- Patrycy Ziółkowski
Systemy dyspersji składają się z dwóch lub więcej związków chemicznych lub prostych substancji, zwanych komponentami systemowymi, rozmieszczonymi między sobą. Tworzą się:
- Faza rozproszona - substancja rozproszona;
- Medium ciągłe - substancja, w której rozproszona jest rozproszona faza.
W zależności od wielkości cząstek fazy rozproszonej istnieją:
- Heterogeniczne (szorstkie) układy dyspersji - cząstki są większe niż 100 nm:
- Zawieszenie - składnik cieczy i stały;
- Emulsja - dwa składniki płynne;
- Aerozol - medium dyspersji to gaz.
- Koloidy - rozmiar cząstek wynosi od 1 do 100 nm;
- Rzeczywiste roztwory - wielkość cząstek jest mniejsza niż 1 nm.

Co to jest koloid?
Roztwory wodne wielu substancji (cukier itp.;. Pierwsze substancje nazywane są krystaloidami, a drugi nazywa się koloidami.
W zależności od tego, w jaki sposób cząsteczki rozproszonej fazy odnoszą się do medium, układy koloidowe są:
- Lyofiliczny - adsorbuj dużą liczbę cząsteczek z pożywki dyspersyjnej (żelatyna, mydła, Fe (OH)3, AL (OH)3);
- Liofobiczne - nie wiążą się ani nie wiążą się z niewielką liczbą cząsteczek z pożywki dyspersyjnej (sole niektórych metali, słabo rozpuszczalne siarczki metalu itp.).
W zależności od struktury cząstek koloidalnych układy koloidowe są podzielone na:
- Powiązane (micelarne) - cząstki są grupami atomów, jonów lub cząsteczek (e.G. chlorek sodu w benzenie);
- Cząsteczki - cząstki są cząsteczkami związku o wysokiej masie cząsteczkowej (e.G. skrobia).
W zależności od charakteru medium koloidy to:
- Hydrosols - rozpuszczalnik to woda;
- Benzenosols - rozpuszczalnikiem jest benzen;
- Etherosols - rozpuszczalnik to eter itp.
Właściwości optyczne koloidów przejawiają się jako kolorowanie, opalescencja i efekt tindalny. Są one spowodowane różnicami w absorpcji i rozproszenia światła z cząstek koloidalnych.
Cząstki koloidalne są większe i cięższe niż jony i większość cząsteczek, więc ich dyfuzja i ciśnienie osmotyczne są niskie.
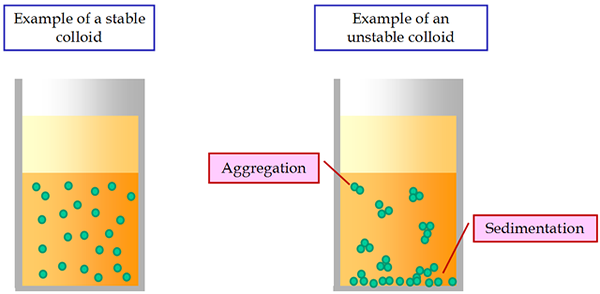
Charakterystyczną kinetyczną właściwością koloidów jest ruch Browna. Systemy koloidalne są mniej stabilne niż w przypadku zwykłych rozwiązań. Pod stałym prądem elektrycznym wszystkie cząstki koloidowe przenoszą się do odpowiedniej przeciwnie naładowanej elektrody. Zjawisko to nazywa się elektroforezą.
Rozwiązania koloidów molekularnych uzyskuje się analogicznie do rzeczywistych roztworów. Po kontakcie fazy rozproszonej rozpuszcza się spontanicznie w rozproszonym pożywce. Rozoleje powiązanych koloidów są uzyskiwane różnymi metodami dyspersji i kondensacji.
- Metody dyspersji - dyspersja materiału do wielkości cząstek koloidalnych w obecności pożywki dyspersyjnej;
- Metody kondensacji - kondensacja (grupowanie) poszczególne cząsteczki, atomy lub jony w cząstki wielkości koloidów.
Co to jest zawieszenie?
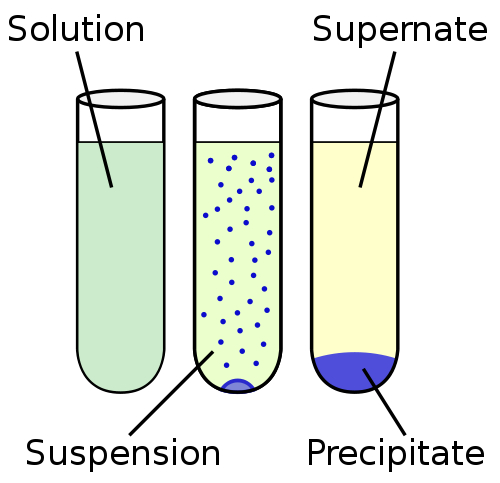
Zawieszenie jest heterogeniczną cieczą, zawierającą nierozpuszczalne cząsteczki stałe, które są wystarczająco duże, aby się uspokoić, ale przez pewien czas występują w objętości macierzy ciekłej. Cząstki są większe niż 100 nm.
Klasyfikacja zawiesin opiera się na fazie rozproszonej i podłożu dyspersji.
Zawieszenie jest bliższe nierozpuszczalności w kontinuum rozpuszczalności. Na drugim końcu kontinuum rozpuszczalności jest roztwór, w którym cząstki są całkowicie mieszane i nie obserwuje się fazy stałej. Kontinuum rozpuszczalności jest ogólnie ułożone w kolejności: nierozpuszczalność, sedymentacja, zawieszenie, koloid i roztwór.
Faza stała zawiesiny jest rozproszona w fazie ciekłej przez mechaniczny proces mieszania za pomocą środka obojętnego lub słabo aktywnego stosowanego jako środek zawieszający. W przeciwieństwie do koloidów, zawiesiny z czasem osadzają się. Przykładem szybko wytrącającego się zawiesiny jest piasek i woda.
Charakterystyczną właściwością zawiesin jest ich niejednorodność optyczna, która wyraża się przez zmętnienie. Zmętnienie jest integralnym zewnętrznym znakiem zawiesiny i jest określany przez obecność nierozpuszczalnych cząstek, które są nieprzepuszczalne do światła. Stopień zmętnienia zawiesin jest inny. Jest to określone przez stężenie fazy zawieszonej i stopień jej dyspersji (wielkość cząstek).
Jedną z najważniejszych cech zawiesin jest ich niestabilność sedymentacji. Jest wyrażany w nieuniknionym osiedleniu zawieszonych cząstek pod wpływem grawitacji. Cząstki mogą samodzielnie się osiedlić, bez trzymania się razem. W takim przypadku istnieje agregatywna stabilność zawieszenia.
Jeśli cząsteczki osadzające się trzymają się pod wpływem sił molekularnych spójności i tworzących się agregatów, wówczas występuje agregacyjna niestabilność zawiesin. Zatem niestabilne sedymentacje zawiesiny mogą być agregatywnie stabilne lub niestabilne.
Czasami w koagulacyjnych zawiesinach powstają duże płatki, które są słabo zwilżone przez ośrodek dyspersji i unoszą się na powierzchni. Zjawisko to nazywa się flokulacją.
Niestabilność sedymentacji zawiesin w praktyce prowadzi do stopniowego zakłócenia jednolitego składu przed całkowitym osadzaniem się fazy nierozpuszczalnej.
Istnieją również zawiesiny, które mogą pozostać w stanie zawieszonym przez długi czas. Nazywane są stabilnymi zawiesinami.
Zawiesiny są uzyskiwane przez różne metody dyspersji i kondensacji.
Różnica między koloidem a zawieszeniem
-
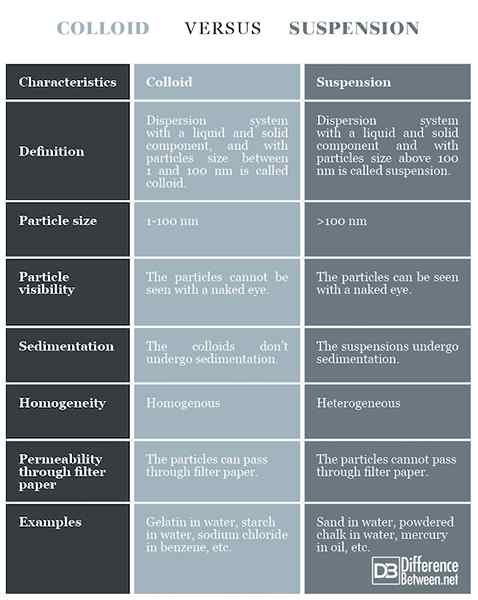
Definicja
Koloid: Układ dyspersji z płynnym i stałym składnikiem, o wielkości cząstek od 1 do 100 nm, nazywa się koloidem.
Zawieszenie: Układ dyspersji z płynnym i stałym składnikiem, o wielkości cząstek powyżej 100 nm, nazywa się zawiesiną.
-
Rozmiar cząsteczki
Koloid: Rozmiar cząstek wynosi 1-100 nm.
Zawieszenie: Rozmiar cząstek jest powyżej 100 nm.
-
Widoczność cząstek
Koloid: Cząstki na kolocie nie można zobaczyć nagim okiem.
Zawieszenie: Cząstki w zawiesinie można zobaczyć nagim okiem.
-
Osadzanie
Koloid: Koloidy nie podlegają sedymentacji.
Zawieszenie: Zawiesiny ulegają sedymentacji.
-
Jednorodność
Koloid: Koloidy są stosunkowo jednorodne.
Zawieszenie: Zawiesiny są heterogeniczne.
-
Przepuszczalność przez papier filtracyjny
Koloid: Cząstki koloidowe mogą przechodzić przez bibułę filtracyjną.
Zawieszenie: Cząstki zawieszenia nie mogą przechodzić przez bibułę filtracyjną.
-
Przykłady
Koloid: Żelatyna w wodzie, skrobi w wodzie, chlorku sodu w benzenu itp.
Zawieszenie: Piasek w wodzie, sproszkowana kreda w wodzie, rtęci w oleju itp.
Wykres porównawczy koloidu i zawieszenia
Podsumowanie koloidu i zawieszenia
- Systemy dyspersji składają się z dwóch lub więcej związków chemicznych lub prostych substancji, zwanych komponentami systemowymi, rozmieszczonymi między sobą. Tworzą zdyspergowaną fazę i ciągłe medium.
- Układ dyspersji z płynnym i stałym składnikiem, o wielkości cząstek od 1 do 100 nm, nazywa się koloidem.
- Układ dyspersji z płynnym i stałym składnikiem, o wielkości cząstek powyżej 100 nm, nazywa się zawiesiną.
- Cząstki na kolocie nie można zobaczyć nagim okiem, podczas gdy cząstki w zawiesinie można zobaczyć nagim okiem.
- Koloidy nie podlegają sedymentacji, a zawiesiny ulegają sedymentacji.
- Koloidy są stosunkowo jednorodne, podczas gdy zawiesiny są heterogeniczne.
- Cząstki koloidowe mogą przechodzić przez bibułę filtracyjną, podczas gdy cząstki zawiesin nie mogą.
- Przykładami koloidów są żelatyna w wodzie, skrobi w wodzie, chlorek sodu w benzenu itp. Przykładami zawiesin są piasek w wodzie, sproszkowana kreda w wodzie, rtęć w oleju itp.

