Różnica między CIS a trans

- 3190
- 667
- Pani — Jóźwiak
Izomeryzm CIS-TRANS polega na możliwości umieszczenia grup podstawników po jednej lub po różnych stronach płaszczyzny podwójnego wiązania lub cyklu niearomatycznego. Izomery CIS-Trans należą do diastereomerów, ponieważ nie są to odbici. CIS i izomery trans znajdują się zarówno wśród związków organicznych, jak i nieorganicznych.
Nomenklatura CIS-Trans opisuje względną pozycję substytutów i nie przedstawia opisu stereochemicznego, jako e, z-nomenklatury, mających zastosowanie tylko dla alkenów.
Oddzielne istnienie cis i izomerów jest możliwe tylko ze względu na wysoką barierę energetyczną obrotu wokół podwójnego wiązania.

Co to jest cis?
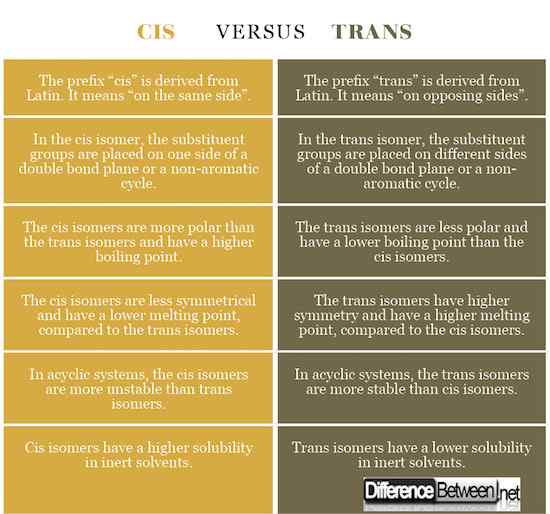
Prefiks „cis” pochodzi z łaciny. Oznacza to „po tej samej stronie”. W izomerze CIS grupy zastępcze są umieszczane po jednej stronie płaszczyzny wiązania podwójnego lub cyklu niearomatycznego.
Izomery CI i trans różnią się ich właściwości fizycznymi, ze względu na nierówność w ogólnym momencie dipolowym i kształcie cząsteczek.
Względna temperatura wrzenia jest określana przez polaryzm. Powoduje zwiększone siły międzycząsteczkowe, co powoduje wzrost temperatury wrzenia. Izomery CIS, które są bardziej polarne niż izomery trans, mają wyższą temperaturę wrzenia. Różnica może być niewielka, jak na przykład w alkenach z łańcuchem prostym. Większą różnicę obserwuje się w substancjach z wiązaniami polarnymi. Przykładem takiej substancji jest 1,2-dichloroeten. Temperatura wrzenia izomeru CIS wynosi 60.3 ° C i jego izomer trans - z 12.8 ° C niższe. Powodem różnicy jest to, że w izomerze CIS dwa momenty dipolowe wiązań polarnych C-Cl. W rezultacie występują międzycząsteczkowe siły dipol-dipolowe, które podnoszą temperaturę wrzenia.
Symetria pozwala na lepsze pakowanie substancji stałych. W wyniku różnej symetrii cząsteczek, izomery CI i trans. Izomery CIS, które są mniej symetryczne, mają niższą temperaturę topnienia, w porównaniu z izomerami trans.
Kolejną cechą izomerów CIS jest to, że mają one wyższe gęstości niż ich odpowiedniki Trans.
Zwykle w systemach acyklicznych izomery CIS są bardziej niestabilne niż izomery trans. Powodem tego jest wzrost niekorzystnej interakcji sterycznej podstawników w izomerach CIS. Zasadniczo izomery CIS mają większą rozpuszczalność w obojętnych rozpuszczalnikach.
Co to jest trans?
Prefiks „trans” pochodzi z łaciny. Oznacza to „po przeciwnych stronach”. W izomerze trans grupy zastępcze są umieszczane po różnych stronach płaszczyzny wiązania podwójnego lub cyklu niearomatycznego.
Temperatura wrzenia izomerów trans jest niższa niż w izomerach CIS. Różnica jest bardziej znacząca w substancjach z wiązaniami polarnymi. W izomerze trans 1,2-dichloroetenu dwa momenty wiązań C-Cl anulują się, a cząsteczka ma zerowy dipol netto. W rezultacie nie ma międzycząsteczkowych sił dipol-dipolowych, które zmniejszają temperaturę wrzenia.
Symetria cząsteczek jest kluczem do oznaczania temperatury topnienia, ze względu na lepsze pakowanie substancji stałych. Przykładami tego są kwas oleinowy (izomer cis) i kwas elaidin (izomer trans). Punkt topnienia izomeru CIS wynosi 13.4 ° C, izomer trans tope w temperaturze 43 ° C. Powodem tego jest to, że izomer trans jest prostszy, pakuje lepiej, a zatem - ma znacznie wyższą temperaturę topnienia.
Izomery trans mają niższe gęstości niż ich odpowiedniki CIS. W systemach acyklicznych izomery trans są bardziej stabilne niż izomery CIS. Zasadniczo izomery CIS mają większą rozpuszczalność w obojętnych rozpuszczalnikach.
Różnica między CIS a trans
-
Definicja CIS i trans
CIS: Prefiks „cis” pochodzi z łaciny. Oznacza to „po tej samej stronie”. W izomerze CIS grupy zastępcze są umieszczane po jednej stronie płaszczyzny wiązania podwójnego lub cyklu niearomatycznego.
Trans: Prefiks „trans” pochodzi z łaciny. Oznacza to „po przeciwnych stronach”. W izomerze trans grupy zastępcze są umieszczane po różnych stronach płaszczyzny wiązania podwójnego lub cyklu niearomatycznego.
-
Polaryzacja i temperatura wrzenia CIS i Trans
CIS: Polaryzacja powoduje zwiększenie sił międzycząsteczkowych, co powoduje wzrost temperatury wrzenia. Izomery CIS, które są bardziej polarne niż izomery trans, mają wyższą temperaturę wrzenia.
Trans: Izomery trans są mniej polarne i mają niższą temperaturę wrzenia niż izomery cis. Różnica jest bardziej znacząca w substancjach z wiązaniami polarnymi.
-
Symetria i temperatura topnienia CIS i Trans
CIS: Izomery cis są mniej symetryczne i mają niższą temperaturę topnienia, w porównaniu z izomerami trans.
Trans: Izomery trans mają wyższą symetrię i wyższą temperaturę topnienia, w porównaniu z izomerami cis.
-
Stabilność i rozpuszczalność CIS i Trans
CIS: W systemach acyklicznych izomery CIS są bardziej niestabilne niż izomery trans. Mają większą rozpuszczalność w obojętnych rozpuszczalnikach.
Trans: W systemach acyklicznych izomery trans są bardziej stabilne niż izomery CIS. Mają niższą rozpuszczalność w obojętnych rozpuszczalnikach.
Podsumowanie cis vs. Trans:
- Izomeryzm CIS-TRANS polega na możliwości umieszczenia grup podstawników po jednej lub po różnych stronach płaszczyzny podwójnego wiązania lub cyklu niearomatycznego.
- Oddzielne istnienie cis i izomerów jest możliwe tylko ze względu na wysoką barierę energetyczną obrotu wokół podwójnego wiązania. Znajdują się zarówno wśród związków organicznych, jak i nieorganicznych.
- Prefiks „CIS” i trans pochodzą z łaciny. CIS oznacza „po tej samej stronie”, trans oznacza „po przeciwnych stronach”.
- W izomerze cis grupy podstawników są umieszczane po jednej stronie, podczas gdy w izomorze trans grupy podstawnikowe są umieszczane po różnych stronach płaszczyzny wiązania podwójnego lub cyklu niearomatycznego.
- Polaryzacja powoduje zwiększenie sił międzycząsteczkowych, co powoduje wzrost temperatury wrzenia. Izomery CIS są bardziej polarne niż izomery trans i mają wyższą temperaturę wrzenia. Różnica jest bardziej znacząca w substancjach z wiązaniami polarnymi.
- Izomery cis są mniej symetryczne i mają niższą temperaturę topnienia, w porównaniu z izomerami trans.
- W systemach acyklicznych izomery CIS są bardziej niestabilne niż izomery trans. Mają większą rozpuszczalność w obojętnych rozpuszczalnikach.